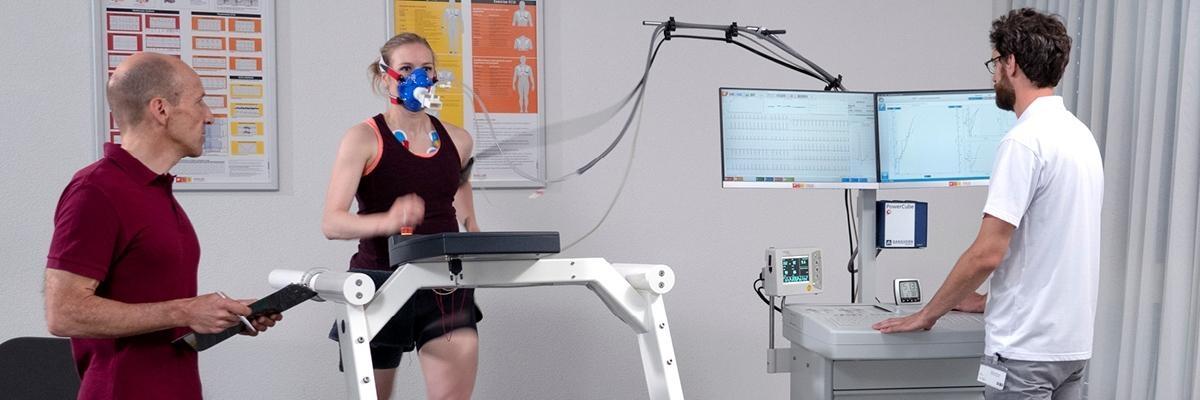
Post Market Surveillance Manager 100%
Baar
Key information
- Publication date:15 October 2025
- Workload:100%
- Contract type:Unlimited employment
- Language:German (Fluent), English (Fluent)
- Place of work:Altgasse 68, 6341 Baar
Die SCHILLER AG ist eine international führende Medtech-Unternehmung im Bereich der Herz- und Lungen-Diagnostik, Patientenüberwachung, Defibrillation, Rettungsmedizin sowie Softwarelösungen für die Medizinbranche. Unsere in der Schweiz entwickelten und gefertigten Produkte werden weltweit erfolgreich in Kliniken und Arztpraxen wie auch von Rettungsgesellschaften eingesetzt.
Zur Verstärkung unseres Teams in der Regulatory Affairs Abteilung suchen wir per sofort oder nach Vereinbarung eine motivierte Persönlichkeit als
Bist Du eine analytisch denkende Person, die gerne im Team arbeitet? Motivieren Dich Herausforderungen und gehst Du diese selbständig und proaktiv an?
Deine Aufgaben
- Koordination aller Aktivitäten im Rahmen der Marktüberwachung nach dem Inverkehrbringen (Trending / PMS)
- Erstellung von PMS-Plänen und -Berichten (PSUR) sowie Organisation und Durchführung von PMS-Reviews gemäss den geltenden Anforderungen
- Analyse und Bewertung von Vorkommnissen zur Sicherstellung der Einhaltung gesetzlicher Vorgaben für auf dem Markt befindliche Medizinprodukte
- Überwachung, Entwicklung und Umsetzung regulatorischer Strategien für zugewiesene Produktprojekte innerhalb interdisziplinärer Produktentwicklungsteams
Dein Profil
- Ausgeprägte analytische und konzeptionelle Denkweise sowie eine selbstständige und proaktive Arbeitsweise
- Abgeschlossenes Studium in einem relevanten Fachgebiet der Medizintechnik (Universität, FH) oder eine vergleichbare Qualifikation durch Berufserfahrung
- Fundierte Erfahrung im Bereich Regulatory Affairs/Qualitätsmanagement für aktive Medizinprodukte
- Sicherer Umgang mit Risikomanagement-Prozessen gemäss geltender Normen und regulatorischer Anforderungen
- Erfahrung in der Marktüberwachung und Bewertung von Vorkommnissen im Rahmen des PMS
- Umfassende Kenntnisse im Meldewesen, einschließlich der Anwendung von IMDRF-Codes
- Sehr gute Kenntnisse der EU-MDR 2017/745 sowie der regulatorischen Anforderungen in UK, CH und den MDSAP-Ländern (z. B. Kanada, USA)
- Sehr gute Sprachkenntnisse in Deutsch und Englisch (Wort und Schrift)
Deine Perspektiven
Freue Dich auf eine spannende und abwechslungsreiche Herausforderung in einem dynamischen, internationalen Arbeitsumfeld. Dich erwartet eine professionelle, innovative und fördernde Arbeitsatmosphäre – eingebettet in die faszinierende Welt der Medizintechnik.
Unsere flexiblen Arbeitszeiten ermöglichen Dir, Deinen Arbeitsalltag individuell zu gestalten. Wir unterstützen Deine berufliche Entwicklung aktiv, indem wir Dir Zugang zu Weiterbildungen und Fachkursen bieten. Zudem profitieren alle SCHILLER AG Mitarbeitende von einem umfassenden Angebot an Benefits.
Bewirb Dich jetzt unter: www.schiller.ch/de/ueber-schiller/karriere, SCHILLER AG, Patricia Luzi, Human Resources, Altgasse 68, 6341 Baar. Wir freuen uns, Dich kennenzulernen!
Für diese Position berücksichtigen wir nur Direktbewerbungen, danke für das Verständnis.
